
PharmaChain: блокчейн в фармацевтической отрасли. Прорывные варианты использования и решения
Некачественные и поддельные лекарственные препараты могут содержать несоответствующие активные ингредиенты, токсичные химические вещества или неизвестные примеси. Их производство может вестись в антисанитарных условиях неквалифицированным персоналом. Так как поддельные лекарства бывают визуально практически идентичны подлинным и их очень трудно отличить, они способны нанести вред пациентам, создать устойчивость к исходному продукту или привести к летальному исходу. По оценкам ВОЗ, растущее количество попадающих в обращение контрафактных и фальсифицированных лекарств ежегодно уносит жизни более миллиона человек во всем мире.
В развивающихся странах проблема контрафакта стоит более остро. Так, во многих странах Азии, Африки и Южной Америки доля поддельных лекарственных средств в общем объеме продаваемой фармацевтической продукции составляет от 10% до 30%. Распространение опасной продукции происходит из-за высокого уровня коррупции и слабозащищенных границ. В США и Европе иная проблема – незарегистрированные онлайн-аптеки, которым удается обходить нормативный контроль. По оценкам ВОЗ, 50% лекарств, приобретаемых через Интернет, являются поддельными12. Рост числа платформ электронной коммерции в сфере фармацевтики расширяет каналы продаж и облегчает процесс вывода на рынок поддельных лекарств, реализуемых по более низким ценам по сравнению с легальными препаратами. Основным фактором, стимулирующим рост обращений в интернет-аптеки, является рост стоимости лекарств.
В результате правительства и регуляторы во всем мире ужесточают свои требования к целостности цепочки поставок в надежде замедлить глобальный поток контрафактных лекарственных средств. Однако, несмотря на крупные международные расследования и массовые изъятия, усиление роли фармкомпаний в обеспечении целостности цепочек поставок лекарств, достижения в области надзора и развитие технологий обнаружения, доля контрафакта все еще остается значительной, и требуются дополнительные меры, чтобы остановить его распространение.
Усиление зависимости от поставщиков и аутсорсинга
По мере усложнения продукции и технологий, а также снижения рентабельности продаж, компании вынуждены все больше полагаться на аутсорсинг13. Если в прошлом различные функциональные элементы отрасли традиционно находились под крышей одной компании, то сегодня вертикально интегрированные цепочки поставок распадаются на отдельные составляющие виды деятельности, которые передаются на аутсорсинг. При этом возрастает сложность управления цепочками поставок, когда сырье, компоненты, готовая продукция и элементы упаковки поступают от разных поставщиков.
Соблюдение требований надлежащей дистрибьюторской
практики (GDP)
GDP (Good Distribution Practice, надлежащая дистрибьюторская практика) – международный стандарт, который устанавливает требования в отношении хранения, транспортировки и дистрибуции лекарственных средств. Для дистрибьюторов и логистических операторов обеспечение выполнения требований GDP является критически важным аспектом выполнения ими обязательств перед партнерами по цепочке поставок. Работа с дистрибьютором или логистическим оператором, не соблюдающим принципы GDP, может создать для фармпроизводителя ряд серьезных проблем. Без гарантий соответствия GDP не может быть уверенности в соблюдении условий хранения, качестве и безопасности лекарственной продукции.
В последнее время в мире растет количество лекарственных средств, для которых в процессе транспортировки и хранения должен быть обеспечен особый температурный режим. Многие иммунобиологические и онкологические препараты требуют поддержания постоянной температуры в диапазоне от 2° C до 8° C. По оценкам экспертов, 20% всех вакцин в мире портятся из-за несоблюдения требуемых условий при транспортировке и хранении. Любой температурный скачок или отклонение от необходимого диапазона может сделать чувствительные препараты не только неэффективными, но и небезопасными для пациентов.
Кроме основного фактора температуры, на качество и безопасность фармакологической продукции способны оказать негативное влияние вибрация, уровень влажности и свет. Поэтому все участники логистической цепи – от производителя до аптеки или медучреждения – должны строго выполнять требования по поддержанию правильной температуры, влажности, давления воздуха и других параметров.
Большое количество посредников между производителем и конечным потребителем усложняет задачу выполнения необходимых требований GDP. Это и многократная перегрузка на различные виды транспорта в разных климатических зонах, и сезонные изменения погоды, когда продукция подвергается значительным температурным изменениям14. В связи с этим во всем мире актуальной является проблема организации перевозок и хранения медицинских препаратов и вакцин в режиме «холодовой цепи».
С развитием технологий мониторинг фармацевтических продуктов улучшился. Сегодня лекарства контролируются по всей цепочке поставок с использованием интеллектуальных устройств интернета вещей (IoT). Но температурные колебания все еще затрагивают значительный объем транспортировки лекарственных средств. Цепочка поставок фармацевтических препаратов требует более совершенных способов мониторинга процесса транспортировки. Если возникает проблема с конкретным продуктом или партией, их крайне сложно изъять. Чтобы улучшить прослеживаемость и процессы возврата, фармацевтическим компаниям необходимо более комплексное и согласованное решение.
Качество данных
В настоящее время цепочки поставок фармацевтических препаратов требуют участия множества сторон, осуществляющих ввод и изменение данных, что сильно влияет на качество данных. В то же время со стороны регуляторов растет внимание к целостности данных как к ключевому показателю надежности цепочки поставок и качества продукции. Участники цепи поставок должны иметь возможность обновлять и обмениваться данными, осуществлять проверку достоверности такой информации, взаимодействовать с национальными и международными системами контроля, транспортными системами и регулирующими органами. Кроме того, участники цепи поставок должны располагать полной информацией о подлинности и качестве фармпрепарата в процессе прохождения товара по ЦП15.
Преимущества использования блокчейна в системах управления цепочками поставок
Для предотвращения проблем, стоящих перед фармацевтической индустрией, необходима эффективная система управления цепочками поставок (УЦП). В качестве наилучшего решения для разработки такой системы может рассматриваться технология блокчейн. Блокчейн представляет собой инновационную альтернативу существующим системам УЦП. В цепочках поставок блокчейн может обеспечить безопасность, более быстрое отслеживание, удаленный мониторинг и аудит, упрощение процессов отзыва и возврата продукции, улучшение финансовых транзакций и усовершенствование контрактов. Реализуя неизменную и прозрачную связь между каждым этапом прохождения продукта по цепочке поставок, блокчейн позволяет создать систему, беспрецедентно упрощающую надзор со стороны регуляторов. Простота аудита и четкий контроль над системой Track&Trace (маркировка и прослеживание) означает гораздо меньшие затраты на защиту потребителей от контрафакта. При полном отслеживании лекарственного препарата с момента его создания до пациента, цепочка поставок может стать целостным, точным, контролируемым и безопасным процессом. Это, в свою очередь, приведет к снижению розничных цен и повышению доверия со стороны потребителей.
Среди потенциальных преимуществ использования блокчейна в системах УЦП можно отметить следующие16,17:
– Улучшенная прозрачность и прослеживаемость. Документирование перемещения продукта по цепочке поставок раскрывает его истинное происхождение и точки соприкосновения. Каждый раз, когда продукт переходит от одного участника ЦП к другому, новые транзакции вносятся в блокчейн. Неизменность блокчейна обеспечивает основу для прослеживания лекарств от производителя до конечного потребителя, идентифицируя, где происходит сбой в цепочке поставок. Хранение всей истории продукта, начиная с его производства до продажи конечному потребителю, позволяет легко выявить его фактическое происхождение и этапы прохождения по цепочке поставок. Производители также могут сократить количество отзывов продукции, предоставляя доступ к своим записям участникам рынка и регулирующим органам.
– Целостность цепочки поставок и повышение доверия. Закрытая система учета в экосистеме обеспечивает надежный доверительный обмен информацией между сторонами. Кроме того, экосистема предоставляет контрольный журнал регистрации событий, удовлетворяющий нормативным требованиям.
– Большая масштабируемость. В систему может быть включено практически любое количество участников.
– Расширенная безопасность. В настоящее время блокчейн является наилучшим вариантом для обеспечения кибербезопасности, и до сих пор в нем не было обнаружено никаких нарушений. Общий неизменяемый реестр с кодифицированными правилами, защищенный методом криптографии, может обеспечить конфиденциальность и безопасность данных, а также позволит снизить необходимость в аудите, требуемом внутренними и нормативными требованиями.
– Целостность данных, сокращение документооборота и административных расходов. Блокчейн предоставляет всем сторонам цепочки поставок доступ к одной и той же информации, потенциально уменьшая ошибки, возникающие при передаче данных. Блокчейн может упростить административные процессы и сократить расходы, обеспечивая эффективный аудит данных цепочки поставок. Процессы, включающие длительные и трудоемкие проверки на соответствие нормативным требованиям, могут быть ускорены с помощью технологии распределенного реестра. Прозрачность может придать больший вес проверкам качества и повысить достоверность данных, которыми обмениваются партнеры по цепочке поставок.
– Смарт-контракты в цепочках поставок18. В контексте цепочки поставок умный контракт может использоваться, например, для безбумажных и безопасных трансграничных транзакций. Для запуска исполнения смарт-контракта (например, для перевода денег, подачи таможенных документов или разблокирования средств) могут использоваться различные устройства Интернета вещей, генерирующие соответствующие условия-триггеры. В зависимости от типа транзакции стороны могут принять решение о заключении традиционного письменного соглашения, при этом смарт-контракты могут использоваться в качестве согласованного механизма для быстрого исполнения платежных и других обязательств в соответствии с условиями, установленными соглашением.
Рассмотрим, как будет работать система управления цепочкой поставок фармацевтической продукции с использованием блокчейна. Цепочка поставок фармпрепаратов может включать множество участников, среди которых поставщики сырья, фармпроизводители, дистрибьюторы-оптовики, аптеки, логистические компании, врачи, конечные пользователи и др.
На рис. 3.1 представлена базовая схема системы управления фармацевтической цепочкой поставок на основе блокчейна. В более расширенном варианте, с учетом отслеживания происхождения сырья для производства готовых изделий, она включает следующие этапы19:
– Каждая партия фармацевтических субстанций/АФИ (активного фармацевтического ингредиента) от верифицирован-ного поставщика проверяется, сериализуется и записывается в блокчейн на уровне исходного сырья.
– Фармпроизводитель присваивает каждому готовому препарату уникальный код, на основе которого вычисляется хеш; информация записывается в блокчейн.
– Оптовый дистрибьютор проверяет происхождение поступившего к нему препарата; транзакция добавляется в блокчейн.
– Фармацевт в аптеке проверяет происхождение лекарства, поставленного оптовиком; транзакция добавляется в блокчейн.
– Пациент/покупатель проверяет происхождение полученного в аптеке препарата; транзакция добавляется в блокчейн.
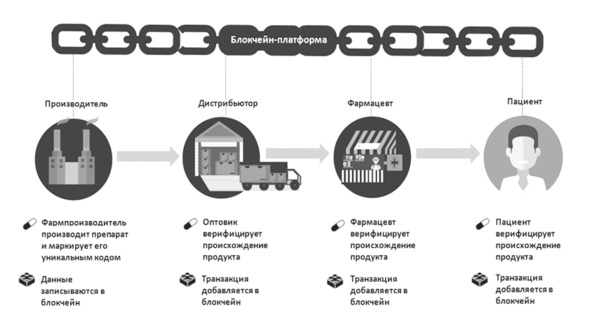
Рис. 3.1. Упрощенная схема системы управления цепочкой поставок на основе блокчейна
С помощью мобильного приложения по идентификационному номеру лекарственного средства каждый участник цепочки поставок может проследить весь путь (историю) препарата и установить его подлинность. Если продукт является подлинным, мобильное приложение покажет всю его историю, а если препарат поддельный – запись не будет отображаться. Как только покупатель убедится в оригинальности лекарства, он может его приобрести20.
В сфере цепочек поставок фармацевтической продукции технология блокчейн может иметь несколько вариантов использования. Одним из них является обеспечение безопасной цепочки поставок и отслеживание (Track&Trace) для противодействия росту контрафактной фармпродукции и связанных с ней затрат. Другой вариант использования – это оптимизация цепочки поставок, которая обеспечивает эффективность, сокращение расходов и возможность контроля уровня запасов, а также скорость и точность кампаний по отзыву препарата из обращения21. Кроме того, применение блокчейна может качественно улучшить мониторинг холодовой цепи, прослеживаемость происхождения и движения фармацевтических субстанций/АФИ (активных фармацевтических ингредиентов) до конечного продукта.
Использование блокчейна для обеспечения безопасной цепочки поставок и отслеживания (Track&Trace)
Блокчейн может рассматриваться как комплексное решение для управления цепочками поставок.
Цепочка поставок в фармацевтике невероятно сложна, в нее вовлечено множество организаций. Все эти игроки могут использовать несовместимые между собой системы. В такой ситуации блокчейн может выступить информационным «мостом»22 и обеспечить инфраструктуру для создания электронной интероперабельной системы. В свою очередь, развертывание блокчейна в качестве инфраструктуры создаст надежную основу для доверия между партнерами. Децентрализованная база данных, доступная всем партнерам по цепочке поставок, улучшит отслеживание лекарств и обнаружение контрафакта.
С помощью блокчейна может быть реализована цифровая верификация авторизованных торговых партнеров (АТП) и обеспечен доступ к данным и системе только для АТП. Возможности блокчейн-системы позволят им эффективно обмениваться данными по каждой транзакции, оперативно реагировать на запросы информации по отслеживанию продукции, проверять идентификаторы продуктов, а также облегчат процедуру расследования инцидентов с подозрительными и некачественными препаратами. Любые расхождения или несоответствия в транзакциях будут отмечены для проверки партнерами по цепи поставок и регулирующими органами23. Блокчейн также может повысить безопасность продукции, ускорив реализацию кампаний по отзыву из обращения некачественной продукции. С помощью оповещений партнеры по сбыту будут предупреждены о проблемах с продукцией в режиме реального времени.
Блокчейн обеспечит неопровержимую запись каждой транзакции в цепочке поставок, предоставляя регуляторам и участникам контрольный след. Кроме того, технология способна защитить данные и систему от фальсификации, злонамеренных атак и взломов, а также обеспечит конфиденциальность коммерческой информации.
По своему характеру технология блокчейн обеспечивает неизменный, общий источник правды и в сочетании с сериализацией и устройствами интернета вещей может рассматриваться в качестве эффективного метода создания более безопасной и надежной цепочки поставок лекарственных препаратов.
Закон о безопасности цепочки поставок лекарств США
В ноябре 2013 года Конгресс США принял Закон о безопасности цепочки поставок лекарственных средств (Drug Supply Chain Security Act, DSCSA)24. Закон отражает растущее внимание правительства США к необходимости усиления регулирующего надзора за контрафактными, краденными, загрязненными или иными небезопасными лекарственными средствами и обеспечения прозрачности сквозной цепочки поставок фармацевтических препаратов. DSCSA устанавливает требования в отношении сериализации, идентификации, отслеживания поставок рецептурных лекарств в США с поэтапным внедрением его норм в течение 10 лет. В законе описываются шаги по достижению интероперабельного электронного отслеживания продукции на уровне упаковки для идентификации и отслеживания определенных рецептурных лекарств в процессе их распространения на территории США. В соответствии с законом, каждая упаковка рецептурных препаратов должна иметь уникальный идентификатор продукта, который может использоваться для отслеживания продукта до его источника. Торговые партнеры в цепочке поставок должны обмениваться информацией о транзакциях, историей транзакций и отчетом о транзакциях по каждому продукту. Эта информация должна предоставляться в электронном формате, совместимом с другими системами в цепочке поставок. В соответствии с DSCSA, все производители, оптовые дистрибьюторы, переупаковщики, 3PL и ретейлеры, а также их торговые партнеры должны быть авторизованными торговыми партнерами (АТП). Если они не будут авторизованы, их доступ к цепочке поставок фармацевтической продукции в США будет строго ограничен или вообще запрещен. Таким образом, во исполнение закона к концу 2023 года в США должна заработать интероперабельная система электронного отслеживания рецептурных фармпрепаратов, обеспечивающая обмен информацией между производителями, оптовыми дистрибьюторами, переупаковщиками и ретейлерами.
Программа пилотов FDA (FDA DSCSA Pilot)
В настоящее время в США запущена инициатива по созданию электронной интероперабельной системы отслеживания рецептурных лекарств, нацеленной на предотвращение попадания на рынок США контрафактных лекарств и нецелевого использования препаратов. Для содействия развитию этой системы в соответствии с требованиями закона DSCSA в феврале 2019 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) учредило программу пилотных проектов25, которая была ориентирована на поиск и рассмотрение любых жизнеспособных технологий и методов, способных обеспечить выполнение требований DSCSA.
Предполагалось, что, поскольку к тому моменту DSCSA действовал уже несколько лет, ведущие компании в сфере поставок лекарств США занимаются изучением всевозможных технологий и разработкой соответствующих решений, и участие в программе пилотов FDA станет для них отличной возможностью протестировать свои наработки. Помимо этого, на тот момент ряд ведущих технологических компаний и стартапов также исследовали возможные комбинации технологий и разрабатывали решения для создания высоконадежной системы, которая позволит компаниям тесно взаимодействовать, сможет легко масштабироваться и обеспечит полное соответствие требованиям DSCSA.
В результате для участия в программе пилотов было отобрано 20 проектов. Минимум семь из них использовали технологические решения на основе блокчейна. Среди них были проекты консорциумов, объединивших ведущих фармацевтических производителей, оптовых дистрибьюторов, аптечные сети и компании технологического сектора: MediLedger, IBM-KPMG-Merck-Walmart, UCLA Health-LedgerDomain, Rymedi, The Optimal Solution, TraceLink и IDLogiq. Цель этих проектов заключалась в установлении полезности блокчейна для повышения прозрачности и прослеживаемости цепочки поставок, а также в определении путей продвижения этой технологии, потенциально изменяющей правила игры в отрасли.
Эти первоначальные пилотные проекты показали положительные результаты и дали все основания полагать, что решение на основе блокчейна способно обеспечить соблюдение DSCSA и может быть использовано для создания интероперабельной, функциональной и конфиденциальной системы отслеживания фармпродукции26. Более подробная информация о консорциуме Mediledger, ведущем участнике FDA DSCSA Pilot, и его решении приводится в главе 9 «Блокчейн-консорциумы в биофармацевтике».
В ходе пилотного проекта консорциума IBM-KPMG-Merck-Walmart было установлено, что прозрачность, обеспечиваемая блокчейном, облегчает участникам фармацевтической цепочки поставок соблюдение DSCSA, предотвращает распространение поддельных лекарств, упрощает процесс отзыва лекарств и многое другое27. Результаты пилотного проекта продемонстрировали, что использование технологии распределенного реестра может значительно сократить время, необходимое для отслеживания отпускаемого по рецепту лекарства – с 16 недель до двух секунд. Пилотное приложение способно предоставить пользователям возможность быстро и эффективно выявлять и сообщать о соответствующем подозрительном или нелегальном лекарственном средстве. Это устраняет разрозненность данных между участниками цепочки поставок и обладает значительным потенциалом для улучшения и ускорения процесса отзыва лекарств.
По оценке IBM28, блокчейн также может повысить безопасность товаров, ускорив реализацию важнейших мер безопасности в цепочке поставок, например, кампаний по отзыву лекарств из обращения. Кроме того, с помощью блокчейна можно будет предупредить партнеров по сбыту о проблемах с продукцией за 10 секунд, тогда как на текущий момент это может занимать до трех дней. Основываясь на результатах моделирования, участники пилотного проекта, использующего технологию блокчейн, подсчитали, что они могут проверить статус продукта всего за несколько секунд. Способность блокчейна помечать лекарство всего через несколько секунд после отзыва потенциально может повысить фармацевтическую безопасность и, по прогнозам, будет иметь далеко идущие последствия для здоровья людей при отслеживании лекарств в регионах, где остро стоит проблема контрафактной или фальсифицированной продукции.
Результаты пилотной программы продемонстрировали, что управляемый блокчейн способен привести сильно фрагментированную цепочку поставок в соответствие с DSCSA. Система может отслеживать движение лекарственных средств, одновременно ограничивая поток конфиденциальной информации и, что наиболее важно, объединять партнеров, которые не взаимодействуют при других условиях29.
Очевидно, что программа пилотных проектов FDA в поддержку реализации норм DSCSA может стать трамплином для массового внедрения блокчейна30. Существует острая необходимость в повышении прозрачности и доверия в цепочке поставок фармацевтических препаратов, учитывая количество задействованных в ней организаций. Поскольку DSCSA затрагивает всех поставщиков в ЦП фармацевтической продукции США, число организаций, которые потенциально могут присоединиться к блокчейн-сетям, огромно. Однако это непростая задача, принимая во внимание сложность организации, управления, развертывания и внедрения интероперабельной системы на основе блокчейна. Кроме того, на пути к широкому внедрению необходимо достичь отраслевого консенсуса. Как известно на примерах других блокчейн-инициатив, сотрудничество внутри отрасли имеет решающее значение. Участие государства в лице регулятора может обеспечить ожидаемый сетевой эффект. В отличие от других отраслей, где законодательное регулирование по-прежнему является серьезным препятствием для внедрения блокчейна, пилотная программа FDA может повысить ожидаемый сетевой эффект блокчейна как основополагающей технологии для цепочки поставок фармацевтической продукции, которая должна быть запущена в США к концу 2023 года. Очевидно, что опыт, накопленный фармацевтической отраслью США, будет экспортироваться за пределы страны и в другие сектора экономики.
Применение блокчейна в системе управления холодовой цепью
Управление холодовой цепью является реальной проблемой общественного здравоохранения. Лекарственные средства – один из самых «капризных» и чувствительных к условиям транспортировки и хранения груз, требующий соблюдения ряда параметров, таких как температура, влажность, давление воздуха и т. д. При несоблюдении какого-либо из них препарат может утратить свои свойства и оказаться бесполезным для конечного потребителя (пациента). В первую очередь, речь идет об обеспечении холодовой цепи – выполнении комплекса мер, направленных на поддержании определенного температурного режима в течение всего периода транспортировки и хранения медикаментов от момента производства до момента применения. Контроль холодовой цепи должен осуществляться на всех этапах движения лекарственных средств.
Сегодня понятие холодовой цепи распространяется на все медицинские препараты, требующие особого температурного режима хранения. При этом особенно строго прописываются требования к соблюдению холодовой цепи в отношении термолабильных лекарственных средств, то есть тех препаратов, которые в случае нарушения требуемого для них температурного режима не только утрачивают свои исходные качества, но и приобретают способность провоцировать нежелательные побочные явления после попадания в организм человека. Известно, что вакцины могут терять свою эффективность вследствие минимальных отклонений от требуемого диапазона температур.

