
Невидимый страж. Как иммунитет защищает нас от внешних и внутренних угроз
Мечников начал свои исследования с детского вопроса: куда исчезают занозы? Каждому из нас случалось загнать под кожу острую щепку. Иногда ее удается вытащить, но частенько она так и остается под кожей. Это место болит несколько дней, а потом заноза словно растворяется и перестает беспокоить. Мечников решил в деталях изучить процесс избавления организма от инородного тела. Но как наблюдать за происходящим, если кожа не прозрачна? Ученый понимал, что защитные силы организма необходимо изучать непосредственно в живом объекте, мертвые ткани для этого не годятся. Он предположил, что подобные защитные механизмы существуют не только у человека, но и у других, более простых животных.
Первым объектом его исследования стали личинки морских звезд, похожие на крошечные стеклянные игрушки. Мечников осторожно втыкал в них шипы розы, а потом в микроскоп следил за тем, что происходит в ране. Уже через несколько минут после повреждения вокруг деревянного острия, словно привлеченные каким-то сигналом, начинали собираться подвижные клетки, похожие на амеб. Они облепляли кусочек дерева, и если он был не слишком большим, то спустя несколько часов от него не оставалось и следа – рана заживала. Так Мечников показал, что в организме животных есть клетки, пожирающие чужеродные частицы. Процесс захвата и переваривания таких частиц он назвал фагоцитозом (от греч. φαγεῖν – пожирать и κύτος – клетка), а сами клетки – фагоцитами.
Это открытие было интересным и важным само по себе, но Мечников предвидел, что значение его может далеко выходить за пределы «прикладного занозоведения». Как врача и ученого его беспокоила проблема инфекционных заболеваний. До открытия антибиотиков оставалось еще несколько десятилетий, и медицина пока мало чем могла помочь больным. За примерами можно было далеко не ходить: первая жена ученого умерла от туберкулеза совсем молодой женщиной. Мечников был в таком отчаянии, что пытался покончить с собой. К счастью для человечества, эта попытка не увенчалась успехом.
Инфекционные заболевания – туберкулез, холера, дифтерия – несли страдания и смерть. Однако Мечников-врач знал, что даже во время самых лютых эпидемий некоторые люди болели легко или не заболевали вовсе. Возможно, открытые им клетки-защитники способны уничтожать не только кусочки дерева, но и микробов? Но как это выяснить? Тут на помощь ученому пришел другой микроскопический обитатель наших водоемов – прозрачный рачок дафния. Он хорошо известен аквариумистам, которые часто разводят дафний на корм рыбам. Эти крохотные ракообразные часто страдают от грибковых инфекций – микозов. Прорастая внутри тела дафнии из спор, грибок убивает животное. Но обязателен ли подобный исход? Видимо, нет, иначе все дафнии давно вымерли бы. Мечников поставил виртуозный эксперимент: он заражал здоровых рачков спорами грибов, а затем под микроскопом наблюдал за тем, что происходит у них в теле. Ученый увидел, что, как и в случае с занозами, споры тут же оказывались атакованными клетками-фагоцитами. Дальнейший ход событий зависел от численности тех и других. Если спор было мало, то фагоциты расправлялись с ними, и дафнии не заболевали. Если же спор было слишком много, то фагоцитов оказывалось недостаточно, чтобы противостоять инфекции, споры прорастали, и рачок погибал. Так была впервые показана роль клеток врожденного иммунитета в защите многоклеточных организмов.
Сегодня мы точно знаем, что именно врожденный иммунитет является первичной защитной системой нашего организма. В том или ином виде он существует у всех многоклеточных животных. Система же приобретенного иммунитета появляется только у позвоночных и является своего рода эволюционной надстройкой над более древними защитными механизмами. Как мы увидим дальше, лимфоциты (Л-клетки) нуждаются в помощи миелоидных клеток и адаптивный иммунитет мало на что способен при повреждении врожденного.
Впрочем, в развитии науки присутствует своя логика, не обязательно совпадающая с логикой эволюционной. Так уж получилось, что на протяжении почти всего XX века открытия Мечникова оставались в тени открытий Эрлиха и его последователей, изучавших адаптивный, то есть приобретенный, иммунитет. Лишь в 2011 году, спустя более чем 100 лет, результаты исследований механизмов врожденного иммунитета вновь привлекли внимание Нобелевского комитета. (Для сравнения: к этому времени было вручено уже по меньшей мере десяток Нобелевских премий за открытия в области иммунитета приобретенного.)
Однако мы в этой книге будем следовать именно биологической, эволюционной логике. Мы начнем наш разговор об иммунитете с рассмотрения наиболее древних механизмов защиты и попытаемся понять, как именно клетки-фагоциты решают три главные иммунологические задачи: распознавание, взаимодействие, уничтожение.
Глава 4
СКАНДАЛЬНЫЙ НОБЕЛЬ
Никогда не скрывал, что академическая наука – клубок друзей и серпентарий единомышленников!
Из бурной дискуссии в интернетеОсень 2011 года в научном сообществе выдалась жаркой, даже можно сказать – скандальной. Едва только Нобелевский комитет объявил имена лауреатов по физиологии и медицине, как в кругах ученых-иммунологов началось настоящее брожение. Нет, важности самого открытия и заслуг Брюса Бётлера и Жюля Офмана[2] никто не отрицал, но в дискуссиях постоянно упоминались имена других исследователей, внесших не менее важный вклад в изучение механизмов врожденного иммунитета. Чаще других называли Чарльза Джейнуэя и Руслана Меджитова. Дошло до того, что группа ученых опубликовала в престижнейшем научном журнале Nature статью о допущенной несправедливости. Голоса в защиту Джейнуэя и Меджитова подняли не какие-то озлобленные неудачники, а самые видные специалисты в области иммунологии. Одним из них был Джеймс Эллисон, который сам несколько лет спустя получил Нобелевскую премию за открытие нового типа иммунотерапии злокачественных опухолей (подробнее о его работе мы поговорим в главе, посвященной раку).
Нобелевский комитет, однако, своего решения не изменил, и Руслан Меджитов (Джейнуэй к тому времени уже умер) Нобелевскую премию так и не получил. Но он узнал, как высоко ценят его собратья-ученые и что они готовы сражаться за признание его заслуг – а это, возможно, даже важнее, чем премия. Такая солидарность в ревнивом мире академической науки встречается редко.
Так что же нового удалось узнать ученым за 100 лет, прошедших после открытия Мечникова, и кто из них на самом деле заслуживал Нобелевскую премию? Я постараюсь ответить на первый вопрос, а что до ответа на второй – решайте сами.
Как было сказано выше, в начале и середине XX века все внимание иммунологов было сосредоточенно на клетках приобретенного иммунитета – лимфоцитах. Но постепенно ученые стали догадываться, что адаптивный иммунный ответ совсем не так самодостаточен, как им казалось раньше. Более того, подавляющее количество многоклеточных животных (в том числе, например, такая многочисленная группа, как насекомые) не имеет его вовсе, однако при этом они как-то справляются с инфекциями. Врожденный иммунитет оказался важнее, чем о нем думали. Перед учеными со всей очевидностью встал один из ключевых вопросов иммунологии: каким образом клетки человека, синтезирующие максимум 20–30 тысяч белков, способны распознавать миллионы антигенов вирусов и бактерий?
Для адаптивного иммунитета ответ на этот вопрос был уже известен: распознавание множества вариантов чужеродных молекул связано с генетически обусловленными перестройками в антигенраспознающих рецепторах Т- и В-клеток. Высокая вариабельность генов этих рецепторов и хитроумные перестройки генного локуса позволяют лимфоцитам синтезировать миллионы разнообразных рецепторов, способных распознавать миллионы чужеродных белков. Ничего похожего в клетках врожденного иммунитета не наблюдается, да и созревание миелоидных клеток идет совсем по другому пути, чем созревание лимфоцитов. А между тем рецепторы клеток врожденного иммунитета, как и любые белки, должны быть закодированы генетически. Но как закодировать распознавание миллионов разных микроорганизмов, которые еще и постоянно изменяются? На это нашего генома просто не хватит!
Между тем фагоциты определенно реагировали на присутствие чужеродных молекул. Так, было известно, что некоторые компоненты микробов, например липополисахарид (ЛПС) из клеточной стенки грамотрицательных бактерий, активируют макрофаги, индуцируя секрецию воспалительных цитокинов, и стимулируют деление В-клеток. Но как?
Эта проблема не давала покоя иммунологу Чарльзу Джейнуэю. В 1989 году он опубликовал статью, в которой раскритиковал современную науку за то, что она направляет все внимание на частности, уклоняясь от действительно фундаментальных вопросов, и предложил собственную теорию врожденного иммунного ответа. Согласно теории Джейнуэя, клетки врожденного иммунитета реагируют на общие сигналы о присутствии чужого – он назвал их образами или паттернами патогенности. В этом их отличие от клеток адаптивного иммунитета, нацеленных на распознавание всего одного или нескольких очень похожих антигенов.
Что имеется в виду? Покинем ненадолго сложный микромир и попытаемся понять идею Дженуэя, используя бытовую аналогию. Предположим, вы выстраиваете систему безопасности вокруг дома, стоящего в густом лесу. Из леса могут прийти волки и медведи, и вы хотите, чтобы система отпугивала их громкими звуками и световыми вспышками. При этом вам совершенно не хочется просыпаться всякий раз, когда в огород проберется мышь или заяц. Стало быть, систему нужно правильно настроить, и тут возможны два подхода. Можно, установив множество скрытых камер, научить систему распознавать конкретных животных и реагировать только в том случае, если в поле зрения камеры появится волк или медведь. Так реагирует адаптивная система, распознавая конкретные молекулы антигенов. Но можно поступить иначе и настроить систему так, чтобы она срабатывала на любой объект размером больше зайца. Второй подход гораздо легче реализовать, хотя у него есть свои издержки: время от времени система будет пугать безобидных косуль или соседа, который решил заглянуть к вам на огонек. Именно так – приблизительно – работает врожденный иммунитет.
Возьмем уже упоминавшийся выше ЛПС. В человеческом организме данная молекула не синтезируется, зато ее производит огромное количество бактерий. Если клетка врожденного иммунитета может распознавать это вещество, то она способна распознать множество болезнетворных бактерий. Ей нет необходимости иметь миллионы рецепторов для миллионов разных молекул, которые могут синтезировать все эти бактерии. Достаточно одного-единственного – распознающего ключевую для всех этих микроорганизмов молекулу. Вот такие молекулы, по мысли Джейнуэя, и были теми самыми образами патогенности, которые распознавались клетками врожденного иммунитета. А поскольку каждый такой образ характерен сразу для целой группы патогенов (в случае с ЛПС это все грамотрицательные бактерии[3]), то в конечном счете и рецепторов к ним требуется не так уж много. Не миллионы, а всего лишь десятки.
Коллеги приняли гипотезу Джейнуэя благожелательно, но без восторга. Генетическая инженерия и молекулярная биология в то время делали еще только первые шаги, возможности их были ограниченны. Как найти потенциальные рецепторы к паттернам патогенности среди тысяч белков, которые присутствуют на поверхности иммунных клеток? Ответа на этот вопрос у Джейнуэя не было, и несколько лет его гипотеза оставалась лишь смелой, но ничем не подтвержденной догадкой.
Глава 5
РЕЦЕПТОРЫ, ПОДОБНЫЕ TOLL
Das war ja toll! (Вот это класс!)
Кристиана Нюсляйн-ФольхардВ то время как в США Джейнуэй ломал голову над загадками врожденного иммунного ответа, за океаном, в Европе, немецкая исследовательница Кристиана Нюсляйн-Фольхард изучала различные мутации у плодовой мушки дрозофилы – излюбленного объекта генетиков еще с начала XX века. В 1985 году среди личинок-мутантов она обнаружила нескольких с недоразвитым брюшком. Кристиана отреагировала на открытие, эмоционально воскликнув: «Das war ja toll!» Именно этим словом «toll» (классный, удивительный) был позднее назван ген, мутация в котором так странно нарушала развитие личинки. В 1995 году Кристиана Нюсляйн-Фольхард была награждена Нобелевской премией за открытие генетических механизмов контроля эмбриогенеза.
Где иммунитет, а где эмбриогенез? Но в организме редкий ген и редкий белок выполняют всего лишь одну функцию. Молекулярная жизнь клетки полна неочевидных, но важных связей и взаимодействий. Вскоре выяснилось, что ген Toll важен не только для эмбрионального развития мушек. Оказалось, что он играет важную роль и в жизни взрослых насекомых. В 1996 году французский исследователь Жюль Офман опубликовал статью, в которой говорилось о том, что сигнальный путь толл-рецептора необходим для защиты дрозофилы от грибковых инфекций. Мушки, имевшие мутации в этом гене, погибали от грибка, в то время как обычные мухи были к нему практически нечувствительны.
Это неожиданное открытие оказалось той последней подсказкой, которую так долго ждал Руслан Меджитов. Молодой ученый прочитал статью Джейнуэя, еще будучи аспирантом МГУ, и идея существования паттернов патогенности настолько захватила его, что он поставил себе цель попасть в лабораторию своего кумира. Когда появилась статья Офмана, Меджитов уже несколько лет работал с Джейнуэем, изучая последовательности генов и кодируемых ими белков, чтобы вычислить первый рецептор врожденного иммунного ответа в геноме человека. Здесь мы сделаем небольшое отступление и поговорим о методах биоинформатики, помогающих ученым предсказывать свойства малоизученных белков и генов, которые их кодируют.
Одним из важнейших событий в биологии ХХ века стало открытие генетического кода – системы правил, по которым последовательность нуклеотидов в ДНК (гене) определяет последовательность аминокислотных остатков в кодируемом ею белке. Другим важным событием было осознание того, что последовательность аминокислотных остатков в белке определяет его структуру, а структура, в свою очередь, определяет функцию.
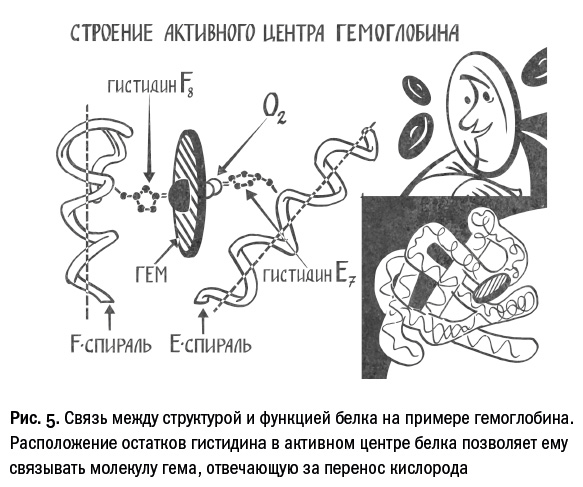
Классическим примером системы «последовательность – структура – функция» является белок гемоглобин, связывающий молекулы кислорода и углекислого газа и осуществляющий их транспорт в нашем организме. Эта функция гемоглобина определяется несколькими остатками аминокислоты гистидина, которые формируют так называемый активный центр белка. Если заменить один из этих гистидинов на остаток какой-то другой аминокислоты, такая молекула не сможет эффективно связывать кислород. Почему именно гистидин? В его состав входит поляризованный атом азота, способный удерживать гем – сложную небелковую молекулу, содержащую атом железа, собственно и связывающий кислород. Однако важен не только химический состав, но и взаимное расположение в пространстве. Остатки гистидина должны находиться на определенном расстоянии друг от друга и под определенными углами. Правильное взаимное расположение обеспечивается стабильностью укладки основных строительных блоков данного белка, которые носят название альфа-спиралей. В свою очередь, эти структуры формируются благодаря чередованию разных типов аминокислот: гидрофильных – любящих воду и гидрофобных – боящихся воды. Таким образом, зная лишь последовательность аминокислот в гемоглобине, мы можем уже довольно много сказать об этом белке. Также вышесказанное позволяет предположить, что гены, обладающие сходными последовательностями, часто кодируют белки с похожими структурами и функциями. Это теоретическое допущение на сегодняшний день имеет множество прямых экспериментальных подтверждений.
Почему это так важно? Дело в том, что прямое определение функции белка и его пространственной структуры продолжает оставаться весьма непростой задачей даже в наши дни. По оценкам ученых, в геноме человека содержится порядка 20 000 генов, кодирующих белки. Но более или менее мы понимаем функции лишь 5000 из них. Что же говорить тогда о миллионах генов, кодирующих белки разных бактерий?
Однако в 1990-х годах определение последовательности генов стало довольно рутинной операцией. Многие тысячи их были уже собраны в первые базы данных – прообразы гигантских биоинформатических хранилищ нашего времени. Специальные программы позволяли сравнивать последовательности генов между собой и находить сходные. Узнав об открытии Офмана, Руслан Меджитов решил искать иголку в стоге сена – проверить, а нет ли среди уже известных человеческих генов похожего на Toll дрозофилы. Конечно, человека и дрозофилу разделяет огромная эволюционная дистанция, но ученые уже знали, что определенные белки, например гистоны, связывающие ДНК в ядре, очень консервативны во всех живых организмах. Возможно, белки иммунной системы также сходны у всех многоклеточных? Во всяком случае, смысл в этих поисках был.
Кто ищет, тот всегда найдет? В науке – отнюдь. Но Меджитову повезло. Он обнаружил в базе данных ДНК последовательность, кодирующую белок, который имел сходство с толл-рецептором дрозофилы. Теперь этот белок известен как толл-подобный рецептор 4 (TLR4). Сходство последовательностей позволяло предположить, что этот белок играет важную роль в защите организма, но само по себе доказательством не являлось. В конце концов, за миллионы лет эволюции, лежащих между человеком и дрозофилой, он мог приобрести другие функции. Чтобы доказать, что этот ген и впрямь вовлечен в иммунный ответ, был необходим эксперимент. На основе исходного гена TLR4 Руслан Меджитов сконструировал искусственный ген, кодирующий мутантный рецептор, который постоянно находится в активном состоянии (природный лиганд, активирующий TLR4, тогда еще не был известен). Мутантный TLR4 поместили в клетки, используя методы генной инженерии, и затем проверили, как отличается активность этих клеток от активности клеток, не подвергшихся генетической трансформации. Оказалось, что гиперактивация сигнальных путей, зависимых от TLR4-рецептора, ведет к усилению производства костимулирующей молекулы В7 и воспалительных цитокинов, необходимых для активации Т-лимфоцитов. Эксперименты Меджитова доказали существование у позвоночных паттерн-распознающих рецепторов, активация которых приводит к инициации адаптивного иммунного ответа. Основное положение теории Джейнуэя было подтверждено. Позже Брюс Бётлер с коллегами показали, что именно рецептор TLR4 связывает липополисахарид клеточных стенок грамотрицательных бактерий.
Конец ознакомительного фрагмента.
Текст предоставлен ООО «ЛитРес».
Прочитайте эту книгу целиком, купив полную легальную версию на ЛитРес.
Безопасно оплатить книгу можно банковской картой Visa, MasterCard, Maestro, со счета мобильного телефона, с платежного терминала, в салоне МТС или Связной, через PayPal, WebMoney, Яндекс.Деньги, QIWI Кошелек, бонусными картами или другим удобным Вам способом.
Сноски
1
Строго говоря, органом иммунной системы является не сам аппендикс, а скопления иммунной (лимфоидной) ткани в его стенках. Аналогичные скопления иммунных клеток в стенках кишечника (Пейеровы бляшки) также относятся к вторичным лимфоидным органам и играют важную роль в настройке иммунной системы.
2
Третьим исследователем, получившим премию в 2011 году, был американский биолог Ральф Стайнман, открывший дендритные клетки. Эта разновидность клеток адаптивного иммунитета играет такую важную роль в настройке иммунного ответа, что ей будет посвящена отдельная глава.
3
Датский ученый-бактериолог Ганс Кристиан Йоахим Грам (1853–1938) занимался систематизацией бактериальных инфекций. Он нашел вещество, которое бактерии одного класса окрашивало в розовый цвет, а другого – нет. В честь ученого те, что окрашивались, названы грамположительными, а те, что оставались бесцветными, – грамотрицательными.
Приобретайте полный текст книги у нашего партнера:




