Синдром Жильбера. Генетический сценарий твоего метаболизма и характера
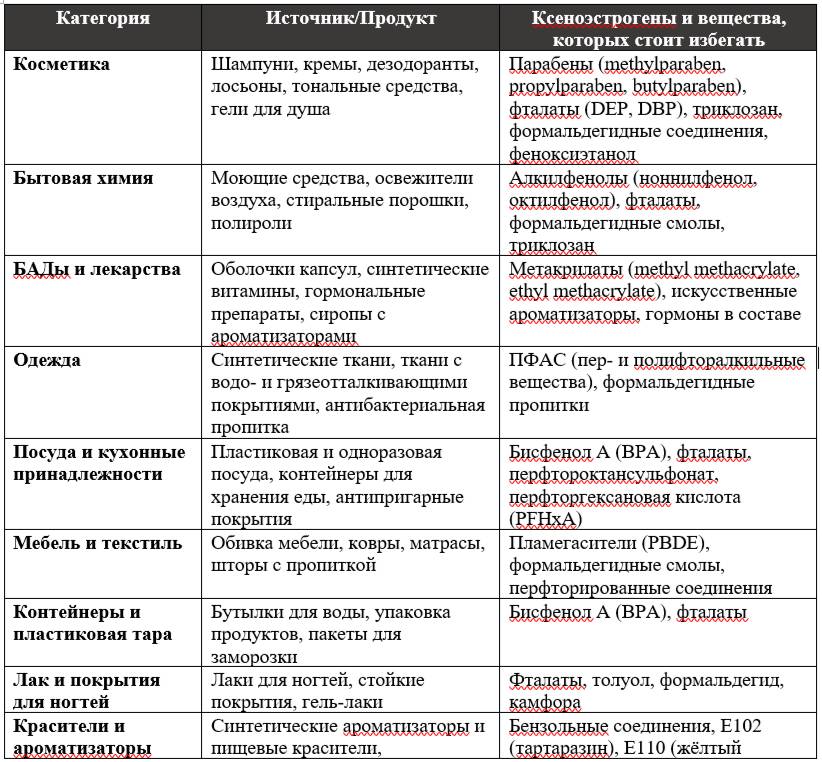
Рисунок №4 «Источники ксеноэстрогенов».

Весь поток токсинов, гормонов и продуктов обмена веществ проходит через один-единственный фермент – глюкуронозилтрансферазу. Всё – и вещества, поступающие из внешней среды, и собственные метаболиты организма – обезвреживаются именно с его участием. Один фермент берёт на себя весь этот колоссальный объём работы. Представьте себе: ежедневно он справляется с бесконечным потоком химических соединений, защищая наш организм.
В условиях современной жизни, когда токсическая нагрузка стремительно растёт – пластик, лекарственные препараты, бытовая химия, избыток гормонов, продукты цивилизации – система детоксикации буквально держится на способности этого фермента вовремя и эффективно нейтрализовать всё, что может нанести вред.
Когда по наследству от обоих родителей передаются две изменённые копии гена UGT1A1, активность этого фермента значительно снижается. В таком случае процесс обезвреживания токсинов замедляется, и это состояние и есть синдром Жильбера. Организм теряет способность эффективно справляться с нагрузкой, и токсины постепенно накапливаются. В результате появляются разнообразные симптомы: хроническая усталость, нарушения работы желудочно-кишечного тракта, гормональные сбои и признаки общей интоксикации.
Чтобы глюкуронозилтрансфераза могла работать полноценно, ей необходим «строительный материал» – глюкуроновая кислота. Именно её фермент присоединяет к токсинам, гормонам и другим соединениям, превращая их в безопасные и готовые к выведению формы.
Глюкуроновая кислота
Глюкуроновая кислота синтезируется в организме из глюкозы, которую мы получаем с пищей. Особенно важную роль здесь играют медленные углеводы – они обеспечивают стабильный, равномерный поток глюкозы без резких скачков уровня сахара в крови. Именно такой стабильный источник глюкозы необходим для постоянного синтеза глюкуроновой кислоты.
В условиях, когда активность фермента снижена по генетическим причинам, как при синдроме Жильбера, мы должны особенно внимательно следить за тем, чтобы этот субстрат поступал в достаточном объёме.
Вот основные источники углеводов и других компонентов, из которых организм производит глюкуроновую кислоту и поддерживает вторую фазу детоксикации:
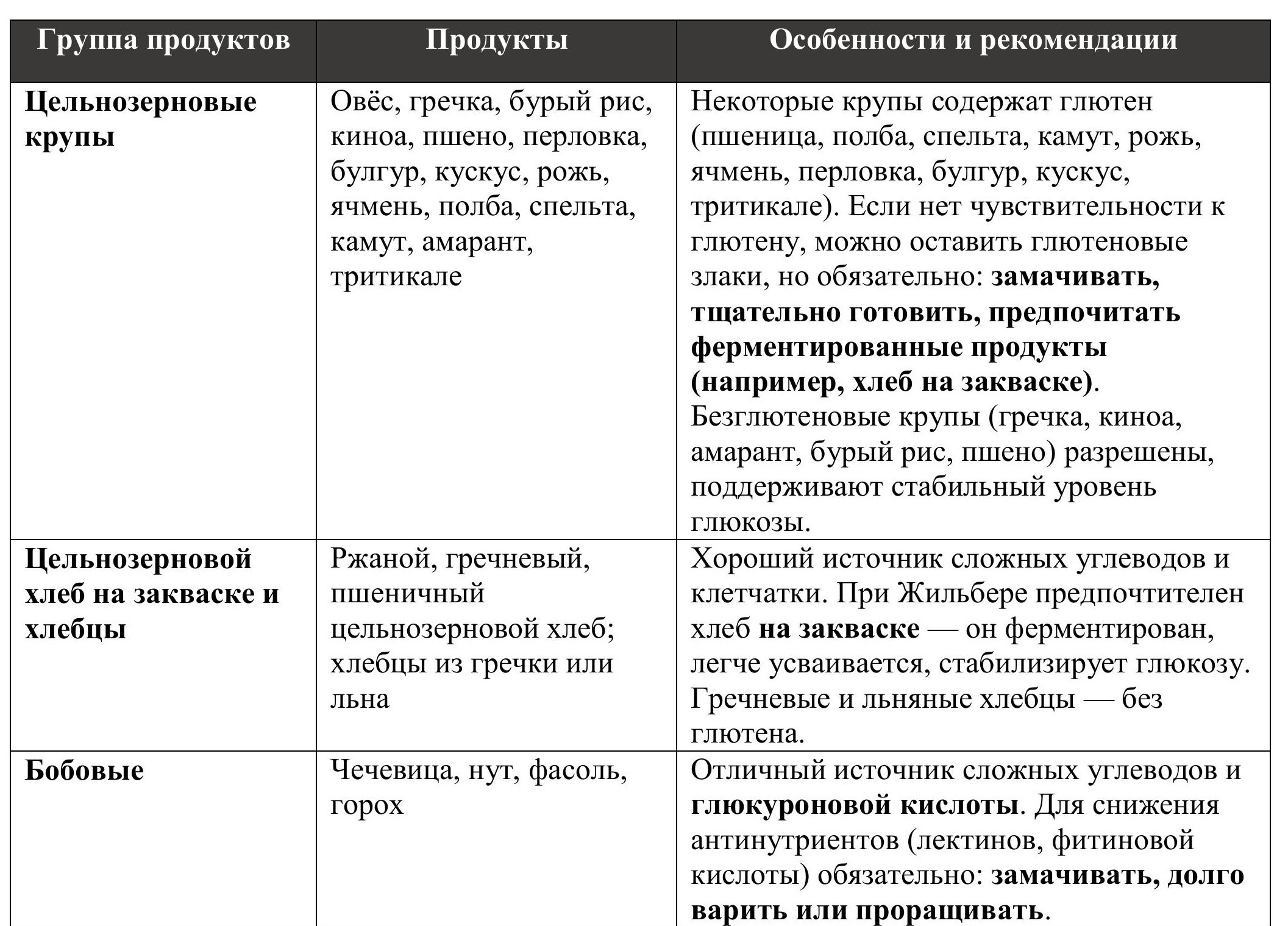
Цельнозерновые крупы: овёс, гречка, бурый рис, киноа, пшено, перловка, булгур, кускус, рожь, ячмень, полба, спельта, камут, амарант, тритикале. Некоторые из этих круп содержат глютен (например, пшеница и её виды – полба, спельта, камут, а также рожь, ячмень, перловка, булгур, кускус, тритикале). При синдроме Жильбера часто нарушена работа ЖКТ, поэтому глютен рекомендуется минимизировать или исключить. Однако если по генам HLA-DQ нет чувствительности к глютену, можно оставить глютеновые злаки в рационе – важно предварительно замачивать их, тщательно готовить и отдавать предпочтение ферментированным продуктам, например, хлебу на закваске. Такие продукты медленно перевариваются и поддерживают стабильный уровень глюкозы.
Цельнозерновой хлеб на закваске и хлебцы: особенно ржаной, гречневый, пшеничный цельнозерновой хлеб, а также хлебцы из гречки или льна. Хороший источник сложных углеводов и клетчатки.
Бобовые: чечевица, нут, фасоль, горох. Отличный источник сложных углеводов и глюкуроновой кислоты. Для уменьшения содержания антинутриентов (лектинов и фитиновой кислоты) рекомендуется тщательно подготавливать бобовые: замачивать их перед приготовлением и подвергать длительной термической обработке.
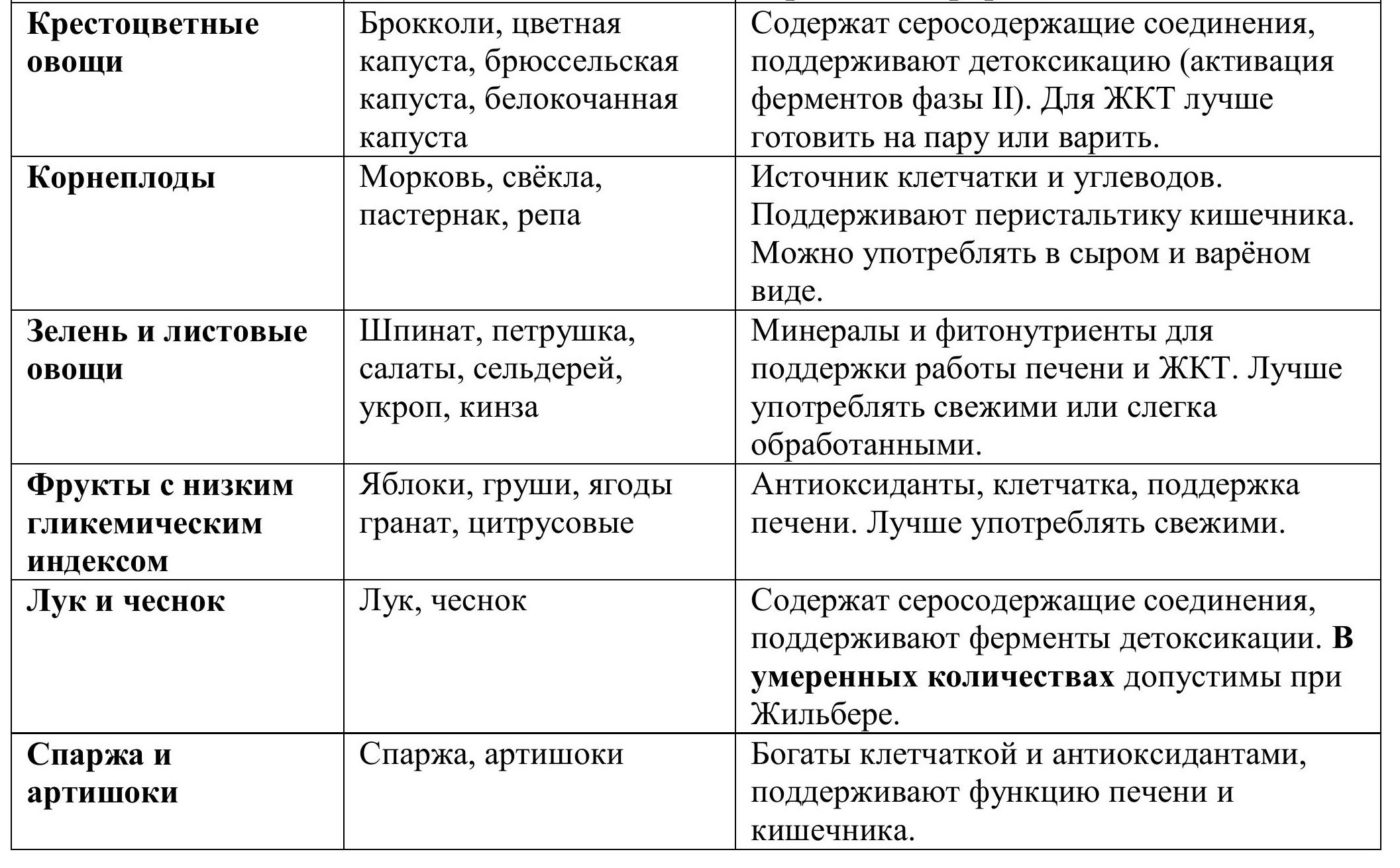
Крестоцветные овощи: брокколи, цветная капуста, брюссельская капуста, белокочанная капуста. Помимо углеводов, содержат серосодержащие соединения, поддерживающие детоксикацию.
Корнеплоды: морковь, свёкла, пастернак, репа. Содержат клетчатку и углеводы.
Зелень и листовые овощи: шпинат, петрушка, салаты, сельдерей, укроп, кинза.
Фрукты с низким гликемическим индексом: яблоки, груши, ягоды (черника, клюква, малина), гранат, цитрусовые (апельсины, лимоны, грейпфруты).
Лук и чеснок: благодаря содержанию серосодержащих соединений также поддерживают работу ферментов детоксикации. В умеренных количествах чеснок допустим при Жильбере, если у человека нет выраженной чувствительности ЖКТ. Лучше использовать его термически обработанным или в минимальных дозах сырого вида (например, в салатах или как добавку к блюдам).
Спаржа и артишоки: богаты клетчаткой и антиоксидантами, дополнительно поддерживают функцию печени и кишечника.
Рисунок №5 «Источники глюкуроновой кислоты».

Если в рационе преобладает кето или низкоуглеводное питание, дефицит углеводов приводит к снижению синтеза глюкуроновой кислоты. При этом организм, сталкиваясь с необходимостью обезвреживать токсины и гормоны, в первую очередь будет направлять все доступные углеводы именно на процессы детоксикации – это приоритетная задача для выживания [6]. Однако на синтез энергии для самого человека углеводов остаётся крайне мало. Именно поэтому у людей с синдромом Жильбера, особенно на фоне дефицита углеводов, часто наблюдается синдром хронической усталости, слабость, эмоциональная и физическая истощаемость, а также зависимость от быстрых углеводов (фрукты, сладости, хлебобулочные изделия).
Чтобы этого избежать, важно наладить регулярное и сбалансированное питание с достаточным количеством медленных углеводов. Интервальное голодание и любые формы длительного голода при синдроме Жильбера не рекомендуются, так как могут спровоцировать всплеск билирубина и ухудшить общее состояние. Также противопоказаны строгие диеты, жёсткие пищевые ограничения и вегетарианство. Такие подходы могут значительно усугубить течение синдрома Жильбера, привести к дефициту белка и ключевых витаминов, нарушить работу ЖКТ и ухудшить функцию детоксикации. Это подтверждают и биографические данные известных личностей. Например, Далай Лама, практикующий вегетарианство и ограниченное питание, нередко отмечал эпизоды слабости и ухудшения самочувствия – подробнее его история описана в главе 21.
Оптимально соблюдать режим не менее 4-х приёмов пищи в день, в каждом из которых должны быть источники белка, клетчатки, медленных углеводов и полезных жиров. Такой подход помогает стабилизировать энергетические уровни и поддерживать полноценную работу фермента глюкуронозилтрансферазы.
Важно учитывать, что глюкуроновая кислота может быть активно потребляема патогенной микрофлорой кишечника. При нарушении баланса микробиоты патогенные бактерии начинают использовать глюкуроновую кислоту для собственных нужд, что дополнительно снижает её доступность для процессов детоксикации [7].
Кроме того, при выраженном дефиците глюкуроновой кислоты организм может начинать забирать её из соединительных тканей – в первую очередь суставов и хрящей. Глюкуроновая кислота является предшественником гиалуроновой кислоты, которая обеспечивает вязкоэластичные свойства синовиальной жидкости и участвует в поддержании структуры хрящевой ткани. Это может проявляться в виде хруста в суставах, гипермобильности, дискомфорта, болей, а в долгосрочной перспективе – привести к ускоренной дегенерации хрящевой ткани [8]. Поэтому важно не только обеспечить поступление медленных углеводов с пищей, но и поддерживать здоровую микрофлору кишечника и общее нутритивное насыщение организма.
Таблица №2: Источники глюкуроновой кислоты. В таблице представлены основные пищевые источники глюкуроновой кислоты.
Глава 3. Генетические нарушения желчеоттока
Одним из ключевых и часто недооценённых проявлений синдрома Жильбера является нарушение желчеоттока. Это наблюдается не только у пациентов с полным синдромом (гомозиготный вариант), но и у носителей одной копии мутации (гетерозиготных носителей).
Ген UGT1A1 отвечает за синтез фермента уридиндифосфат-глюкуронозилтрансферазы. В норме его генотип обозначается как (TA)6/(TA)6, а при наличии синдрома Жильбера всего встречается вариант (TA)7/(TA)7 – это полная форма синдрома. Носительство одной копии мутации – (TA)6/(TA)7 – проявляется мягче, уровень билирубина в таких случаях, как правило, остаётся в пределах нормы и может повышаться только на фоне провоцирующих факторов (стресс, интоксикации, ОРВИ, менструация). Однако нарушение желчеоттока и замедленный процесс детоксикации токсинов присутствуют стабильно у носителей, независимо от провокаций.
При снижении активности фермента UGT1A1 нарушается нейтрализация метаболитов, включая билирубин и продукты обмена гормонов и токсинов. Эти вещества накапливаются и оказывают влияние на свойства желчи. Желчь становится густой, вязкой, приобретает "замазкообразную" консистенцию и плохо оттекает. Это состояние известно, как дискинезия желчевыводящих путей и часто сопровождается застойными явлениями, формированием сладжа (песка) и даже желчных камней [9]. Однако нередко при УЗИ может наблюдаться нормальная картина или выявляться перегиб протоков, что свидетельствует об изменении давления и деформации желчевыводящих путей вследствие нарушения оттока желчи.
Нарушение желчеоттока влечёт за собой:
•
Дефицит жирорастворимых витаминов (A, D, E, K), необходимых для нормального обмена веществ, иммунной функции и здоровья костей. Желчь необходима для всасывания этих витаминов в кишечнике.
•
Снижение усвоения важных нутриентов: железа, кальция, цинка, магния, жирных кислот. Желчь участвует в их эмульгировании и подготовке к всасыванию.
•
Нарушение переваривания жиров. Желчь эмульгирует жиры, подготавливая их к расщеплению ферментами поджелудочной железы.
•
Усиление дисбиоза кишечника из-за застойной желчи. Желчь обладает антисептическим и противомикробным действием, а при её застое микробиота смещается в сторону патогенной.
•
Повышение вероятности паразитарных инвазий. Желчь обладает антисептическим и противопаразитарным действием, а её застой создаёт благоприятные условия для роста и размножения паразитов.
•
Повышенную нагрузку на печень. Не вовремя выведенные токсины и метаболиты возвращаются в кровоток, снова циркулируя и усиливая нагрузку на печень.
•
Развитие дисбаланса жирных кислот и холестерина. Желчь участвует в их переваривании и всасывании, а нарушение этого процесса способствует дисбалансу липидного обмена и увеличивает риски атеросклероза.
•
Нарушение работы поджелудочной железы, вплоть до развития панкреатита. Желчь и сок поджелудочной железы выделяются синхронно, нарушение одного процесса отражается на другом.
Кроме того, желчь выполняет функцию выведения гормонов и токсинов. Если её отток нарушен:
•
Нарушается выведение избытка эстрогенов – повышается риск пролиферативных заболеваний (миомы, мастопатия, эндометриоз), так как большая часть эстрогенов выводится именно с желчью.
•
Задерживаются метаболиты кортизола – проявляется повышенная тревожность, склонность к психоэмоциональному напряжению, формируется типичный "желчный" психотип.
Мутация гена UGT1A1 и связанное с ней снижение активности глюкуронозилтрансферазы являются ведущим фактором в регуляции желчеоттока и обменных процессов. При этом нарушение желчеотделения становится замкнутым кругом, усугубляя дефициты и перегружая детоксикационные системы организма.
Глава 4. Синдром Жильбера: Эволюционные преимущества
Синдром Жильбера (СЖ) – одно из наиболее распространённых наследственных состояний. По моей практике, почти каждый второй человек является либо носителем, либо имеет выраженные проявления синдрома. Официальные данные подтверждают его высокую распространённость: среди европейцев частота встречаемости составляет 2–5%, среди азиатов – около 3%, среди африканцев – до 36%. В России, по данным некоторых исследований, синдром Жильбера выявляется у каждого седьмого россиянина, что составляет около 14% населения. Жильбериков действительно много, и этому есть эволюционное объяснение.
Почему данная мутация закрепилась в процессе эволюции?
На первый взгляд, наличие синдрома Жильбера кажется маловыгодным: нарушение работы фермента уридиндифосфат-глюкуронозилтрансферазы (UGT1A1) приводит к повышению билирубина и снижает эффективность детоксикации. Однако, если углубиться в биохимию и учесть условия, в которых формировался человек как вид, становится понятно, что это состояние имело ряд преимуществ, важных для выживания.
Эволюция закрепляет те признаки, которые повышают шансы на выживание в условиях среды. В доиндустриальную эпоху ключевыми факторами угрозы были инфекции, воспалительные процессы и травмы. Организм нуждался в мощной системе защиты от окислительного стресса и свободных радикалов. Здесь и вступал в игру билирубин.
Потенциальные эволюционные преимущества синдрома Жильбера:
Антиоксидантные свойства билирубина:
Билирубин является мощным эндогенным антиоксидантом, способным эффективно нейтрализовать свободные радикалы и останавливать цепные реакции перекисного окисления липидов. Исследования показали, что по эффективности он превосходит многие известные антиоксиданты, включая витамин Е. Билирубин действует в паре с ферментом биливердинредуктазой, создавая цикл восстановления, который позволяет ему многократно участвовать в обезвреживании активных форм кислорода. Это снижает риск окислительного повреждения тканей, особенно в условиях инфекций, воспалений и стресса, и могло давать носителям СЖ эволюционное преимущество, увеличивая их выживаемость [10].
Противовоспалительное и иммуномодулирующее действие:
Билирубин способен снижать активность воспалительных процессов и предотвращать чрезмерную активацию иммунной системы. Механизм этого действия связан с его влиянием на ключевые сигнальные пути воспаления. В частности, билирубин подавляет активацию NF-κB – одного из главных регуляторов воспалительного ответа, а также снижает экспрессию провоспалительных цитокинов, таких как TNF-α и IL-6. Кроме того, билирубин активирует антиоксидантный путь Nrf2, что способствует снижению окислительного стресса и дальнейшему контролю воспаления. Эти свойства особенно важны при хронических инфекциях и аутоиммунных состояниях, где чрезмерная иммунная активность может нанести вред организму [11].
Снижение риска сердечно-сосудистых заболеваний:
Установлено, что люди с синдромом Жильбера имеют значительно более низкий риск развития атеросклероза и ишемической болезни сердца. Это связано с антиоксидантным действием билирубина, который препятствует окислению липидов и образованию атеросклеротических бляшек в сосудах. В эпоху, когда рацион человека был беден антиоксидантами, а доступ к растительной пище и витаминам был ограничен, такая встроенная защита оказывалась важным эволюционным преимуществом, помогая сохранять здоровье сосудов и снижать риски преждевременной смертности от сердечно-сосудистых заболеваний [12].
Более высокая устойчивость к инфекциям:
Некоторые исследования показывают, что билирубин обладает выраженной противовирусной активностью. В частности, он способен снижать репликацию вирусов, таких как вирус простого герпеса и энтеровирусы, активируя защитные клеточные механизмы, включая выработку оксида азота и ключевых сигнальных путей. В условиях, когда у предков не было доступа к антибиотикам и противовирусным средствам, такие природные механизмы защиты были критически важны для выживания [13].
Потенциальное влияние на продолжительность жизни:
Наблюдения и исследования всё чаще подтверждают: синдром Жильбера – это не просто доброкачественная особенность обмена веществ, а потенциальное биологическое преимущество. Люди с этим синдромом, имея умеренно повышенный уровень билирубина, демонстрируют признаки здорового старения и реже сталкиваются с заболеваниями, связанными с хроническим воспалением. Билирубин, обладая выраженной антиоксидантной активностью, защищает клетки организма от окислительного стресса – ключевого фактора преждевременного старения и развития так называемых «болезней цивилизации».
Влияние билирубина на организм выходит за рамки простой антиоксидантной защиты. Исследования показывают, что он активно участвует в регуляции клеточных процессов, поддерживая баланс между воспалением, метаболизмом и иммунным ответом. Такой комплексный эффект объясняет, почему при синдроме Жильбера наблюдается снижение рисков сердечно-сосудистых, аутоиммунных и нейродегенеративных заболеваний [14].
С эволюционной точки зрения, носительство мутации, характерной для синдрома Жильбера, давало определённые преимущества. В условиях естественного отбора, когда организму необходимо было справляться с инфекциями, воспалениями и ограниченными ресурсами, способность удерживать билирубин на повышенном уровне обеспечивала дополнительную защиту. Именно благодаря этим качествам мутация сохранилась и закрепилась в популяции.
Конечно, характер угроз для организма существенно изменился. В прошлом основными рисками были инфекции и травмы— всё, что вызывало острое воспаление и окислительный стресс. В этих условиях умеренно повышенный билирубин обеспечивал естественную защиту, помогая организму справляться с воспалительными процессами и повреждениями тканей. Сегодня же на первый план вышли другие факторы: хронический стресс, токсические нагрузки, избыток медикаментов и высококалорийная пища. Однако, если при синдроме Жильбера поддерживать центральное слабое звено – детоксикацию, желчеотток и здоровье ЖКТ, эта особенность продолжает работать как природный антиэйдж-ресурс, защищая от «заболеваний цивилизации» способствуя долголетию [15].
Рисунок №6 «Эволюционные преимущества синдрома Жильбера».

Глава 5. Психоэмоциональные особенности
Психоэмоциональный портрет человека с синдромом Жильбера нередко характеризуется особыми чертами. Повышенная тревожность, панические атаки, чувствительность к стрессу, склонность к раздражительности и эмоциональная неустойчивость – эти особенности проявляются настолько часто, что невольно задаёшься вопросом: не случайность ли это? Если копнуть глубже, станет ясно, что причины кроются не только в характере или внешних обстоятельствах, но и буквально «зашиты» в биохимии обменных процессов. Разберём по порядку, какие именно механизмы стоят за формированием так называемого «желчного психотипа».
Влияние неконъюгированного билирубина на нервную систему
Ключевым биохимическим изменением при синдроме Жильбера является накопление неконъюгированного билирубина. Этот тип билирубина обладает выраженными липофильными свойствами, что позволяет ему проникать сквозь гематоэнцефалический барьер и вступать в контакт с клеточными мембранами нейронов [16].
Дальнейшее взаимодействие билирубина с нервной тканью запускает целый каскад нарушений:
•
Происходит повреждение мембран нейронов.
•
Нарушаются функции митохондрий, что снижает энергетическое обеспечение нервных клеток.
•
Ингибируется синтез белка, а также ионный транспорт, критически важный для нейрональной проводимости.
Эти процессы приводят к дисфункции нейронов, что может проявляться в виде неврологических и психоэмоциональных симптомов. Но воздействие билирубина не ограничивается только структурными нарушениями. Всё больше данных указывает на его участие в тонких регуляторных механизмах. В частности, уровень неконъюгированного билирубина рассматривается как возможный биомаркер предрасположенности к определённым психическим расстройствам, особенно в шизофреническом спектре [17, 18]. Исследователи отмечают, что билирубин может влиять на воспалительные процессы, а также обмен нейромедиаторов, таких как дофамин и серотонин, играющих ключевую роль в формировании эмоционального фона, стрессоустойчивости и общего психического состояния. Таким образом, продукты обмена билирубина могут быть токсичными не только на физическом уровне, но и на психоэмоциональном, влияя на качество жизни пациентов с синдромом Жильбера.
Нарушение инактивации стероидных гормонов
Следующим ключевым звеном является участие печени в метаболизме стероидных гормонов. В норме печень эффективно инактивирует избыточные количества кортизола, эстрогенов, прогестерона и тестостерона. При синдроме Жильбера, на фоне общей недостаточности детоксикационной функции печени, процессы инактивации замедляются, что приводит к накоплению этих гормонов в организме [19].
Рассмотрим наиболее значимые последствия этого накопления:
• Кортизол: хронически повышенный уровень кортизола, известного как "гормон стресса", способствует развитию тревожности, эмоционального напряжения, расстройств сна и ухудшения когнитивных функций.
• Эстрогены: избыто к этим гормонам связан с повышенной раздражительностью, склонностью к депрессивным состояниям, мигреням и снижением либидо.
• Прогестерон: дисбаланс прогестерона проявляется перепадами настроения, бессонницей, снижением стрессоустойчивости.
• Тестостерон и его метаболиты: накопление тестостерона может провоцировать импульсивные реакции, агрессивность, раздражительность, что в долгосрочной перспективе приводит к эмоциональному истощению.
Нарушение метаболизма гормонов создаёт мощный фон для формирования характерного эмоционального профиля. Такой фон характеризуется чрезмерной чувствительностью к стрессам, повышенной тревожностью, эмоциональной нестабильностью и сниженной способностью к восстановлению после психоэмоциональных нагрузок. Человек становится более уязвимым к внешним воздействиям, легче выходит из равновесия, острее реагирует на раздражители и дольше возвращается в состояние внутреннего комфорта. Постепенно это отражается на общем качестве жизни – снижается концентрация, ухудшается сон, нарастают ощущения усталости и внутреннего напряжения.
Токсичные метаболиты и синдром хронической усталости
Одним из ярких проявлений синдрома Жильбера, помимо эмоциональной нестабильности и тревожности, становится хроническая усталость. Это состояние не ограничивается банальным чувством усталости после нагрузки – оно носит перманентный характер и нередко сопровождается снижением уровня энергии, ухудшением качества сна, раздражительностью и трудностями в концентрации. Эти проявления логично дополняют общую картину биохимических нарушений, происходящих при синдроме Жильбера. Причины хронической усталости у таких пациентов многоуровневы и тесно связаны с нарушением обменных процессов.
Во-первых, значительная часть глюкозы, поступающей в организм, перераспределяется в пользу синтеза глюкуроновой кислоты. Этот процесс необходим для связывания и обезвреживания неконъюгированного билирубина и других токсичных метаболитов. Однако, при синдроме Жильбера, когда функция конъюгации нарушена, печень вынуждена работать в усиленном режиме, потребляя больше ресурсов. Глюкоза активно вовлекается в процесс детоксикации, что снижает её доступность для производства АТФ и обеспечения энергетических потребностей тканей. На фоне дефицита доступной энергии человек начинает испытывать постоянное чувство истощения, не проходящее даже после отдыха [20].
Во-вторых, негативное влияние оказывает и сам билирубин. Как известно, он обладает липофильными свойствами и способен проникать через гематоэнцефалический барьер, оказывая воздействие на клетки мозга. Одним из таких воздействий является нарушение функций митохондрий. Снижение эффективности энергетического обмена на уровне клеток приводит к снижению толерантности к физическим и умственным нагрузкам [21].
В-третьих, хронический метаболический стресс сопровождается активацией гипоталамо-гипофизарно-надпочечниковой системы. Постоянное пребывание организма в состоянии мобилизации поддерживает высокий уровень кортизола и других стрессовых гормонов, что ещё сильнее истощает энергетические ресурсы и способствует формированию синдрома хронической усталости [22].